La Tabla Periodica
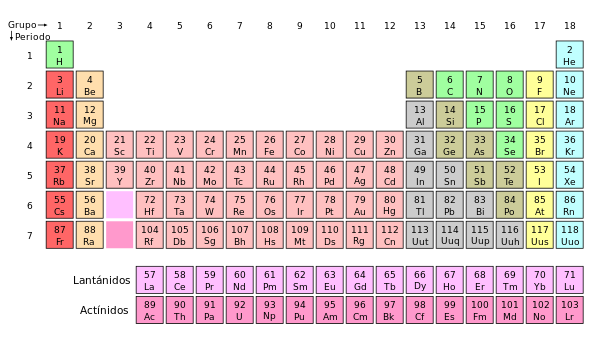
La tabla periódica de los elementos clasifica, organiza y distribuye los distintos elementos quimicos
conforme a sus propiedades y características; su función principal es establecer un orden específico agrupando elementos.
Suele atribuirse la tabla a Dmitri Mendeléyev, quien ordenó los elementos basándose en sus propiedades químicas, si bien Julius Lothar Meyer, trabajando por separado, llevó a cabo un ordenamiento a partir de las propiedades físicas de los átomos. La estructura actual fue diseñada por Alfred Werner a partir de la versión de Mendeléyev. En 1952, el científico costarricense Gil Chaverri (1921-2005) presentó una nueva versión basada en la estructura electrónica de los elementos, la cual permite ubicar las series lantánidos y los actínidos en una secuencia lógica de acuerdo con su número atómico.
Descubrimiento de los elementos:
Aunque algunos elementos como el oro (Au), plata (Ag), cobre (Cu), plomo (Pb) y mercurio
(Hg) ya eran conocidos desde la antigüedad, el primer descubrimiento
científico de un elemento ocurrió en el siglo XVII, cuando el alquimista
Henning Brand descubrió el fósforo (P).
En el siglo XVIII se conocieron numerosos nuevos elementos, los más
importantes de los cuales fueron los gases, con el desarrollo de la química neumática: oxígeno (O), hidrógeno (H) y nitrógeno (N). También se consolidó en esos años la nueva concepción de elemento, que condujo a Antoine Lavoisier
a escribir su famosa lista de sustancias simples, donde aparecían 33
elementos. A principios del siglo XIX, la aplicación de la pila
eléctrica al estudio de fenómenos químicos condujo al descubrimiento de
nuevos elementos, como los metales alcalinos y alcalino–térreos, sobre
todo gracias a los trabajos de Humphry Davy. En 1830 ya se conocían 55 elementos. Posteriormente, a mediados del siglo XIX, con la invención del espectroscopio, se descubrieron nuevos elementos, muchos de ellos nombrados por el color de sus líneas espectrales características: cesio (Cs, del latín caesĭus, azul), talio (Tl, de tallo, por su color verde), rubidio (Rb, rojo), etc.
Los pesos atómicos
A principios del siglo XIX, John Dalton (1766–1844)
desarrolló una concepción nueva del atomismo, a la que llegó gracias a
sus estudios meteorológicos y de los gases de la atmósfera. Su principal
aportación consistió en la formulación de un "atomismo químico" que
permitía integrar la nueva definición de elemento realizada por Antoine Lavoisier (1743–1794) y las leyes ponderales de la química (proporciones definidas, proporciones múltiples, proporciones recíprocas).
Dalton empleó los conocimientos sobre proporciones en las que
reaccionaban las sustancias de su época y realizó algunas suposiciones
sobre el modo como se combinaban los átomos de las mismas. Estableció como unidad de referencia la masa
de un átomo de hidrógeno (aunque se sugirieron otros en esos años) y
refirió el resto de los valores a esta unidad, por lo que pudo construir
un sistema de masas atómicas relativas. Por ejemplo, en el caso del
oxígeno, Dalton partió de la suposición de que el agua era un compuesto
binario, formado por un átomo de hidrógeno y otro de oxígeno. No tenía
ningún modo de comprobar este punto, por lo que tuvo que aceptar esta
posibilidad como una hipótesis a priori.
Dalton sabía que una parte de hidrógeno se combinaba con siete partes
(ocho, afirmaríamos en la actualidad) de oxígeno para producir agua.
Por lo tanto, si la combinación se producía átomo a átomo, es decir, un
átomo de hidrógeno se combinaba con un átomo de oxígeno, la relación
entre las masas de estos átomos debía ser 1:7 (o 1:8 se calcularía en la
actualidad). El resultado fue la primera tabla de masas atómicas
relativas (o pesos atómicos, como los llamaba Dalton), que fue
posteriormente modificada y desarrollada en los años posteriores. Las
inexactitudes antes mencionadas dieron lugar a toda una serie de
polémicas y disparidades respecto a las fórmulas y los pesos atómicos, que solo comenzarían a superarse, aunque no totalmente, en el congreso de Karlsruhe en 1860.
Metales, no metales, metaloides y metales de transición
La primera clasificación de elementos conocida fue propuesta por Antoine Lavoisier, quien propuso que los elementos se clasificaran en metales, no metales y metaloides o metales de transición.
Aunque muy práctica y todavía funcional en la tabla periódica moderna,
fue rechazada debido a que había muchas diferencias tanto en las propiedades físicas como en las químicas.